L’horloge épigénétique est un biomarqueur du vieillissement
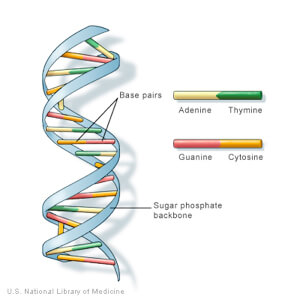
Les altérations épigénétiques, qui constituent une des neuf grandes causes du vieillissement, ont été largement étudiées au cours des dix dernières années. Leur étude approfondie a permis de comprendre les modifications liées à l’âge qui touchent différents mécanismes épigénétiques, à savoir la méthylation de l’ADN, les modifications d’histones et le remodelage chromatinien. La méthylation de l’ADN est un processus lors duquel des groupes méthyles (CH3) se greffent sur des sites spécifiques de l’ADN, condensant ainsi la chromatine et empêchant l’expression de gènes. Les sites spécifiques ciblés par la méthylation sont les cytosines (une des quatre bases de l’ADN) appartenant à des dinucléotides CpG (une cytosine suivie d’une guanine dans la chaîne nucléotidique de l’ADN). Ces méthylations ont lieu naturellement et permettent la régulation de l’expression génique. Cependant, avec l’âge, des altérations de méthylation peuvent apparaître, que ce soit sous forme d’une hyperméthylation ou d’une hypométhylation. Ces modifications de l’état de méthylation d’un gène vont pouvoir être mesurées, constituant ainsi des marqueurs biologiques du vieillissement. La variation de ces phénomènes épigénétiques au cours du vieillissement est appelée horloge épigénétique et permet d’évaluer notre âge biologique [1], qui diffère souvent de notre âge chronologique. Mesurer l’âge biologique permettrait de mesurer le vieillissement de manière beaucoup plus juste, et ouvre de nouvelles pistes thérapeutiques contre le vieillissement.
Aujourd’hui, la métrologie du vieillissement est une science grandissante dont les biomarqueurs sont de plus en plus fiables. Il a été rapporté que l’horloge épigénétique est le biomarqueur le plus prometteur pour estimer l’âge biologique [2]. Dans la lutte contre le vieillissement, étudier les divergences d’âges biologiques entre individus du même âge chronologique pourrait aider à comprendre l’influence des facteurs de stress internes et environnementaux sur le vieillissement [1]. Développer ce marqueur puissant permettra de comprendre, ralentir, arrêter ou reverser le vieillissement [1].
Le principe de l’horloge épigénétique
L’horloge épigénétique est basée sur les modifications du profil de méthylation de l’ADN. On dénombre 28 millions de dinucléotides CpG dans le génome humain [3] dont plusieurs millions ont un profil de méthylation altéré avec l’âge. Plusieurs ensembles regroupant des dizaines voire des centaines de ces sites CpG ont été construit et étudiés pour créer un estimateur de l’âge biologique : l’horloge épigénétique.

L’horloge épigénétique permet de déterminer l’âge biologique de nos cellules, nos tissus et nos organes. L’âge estimé par l’horloge épigénétique est aussi appelée l’âge épigénétique ou “DNAm Age”. L’horloge épigénétique donne également lieu à un autre concept : l’accélération du vieillissement (age acceleration), une mesure correspondante à la différence entre l’âge prédit (âge biologique) par l’horloge épigénétique et l’âge chronologique. Une étude allemande effectuée sur une grande population de personnes âgées a notamment associé le développement de cancers et une augmentation de la mortalité liée aux maladies cardiovasculaires avec l’accélération du vieillissement [4].
Les différentes horloges épigénétiques

Il existe aujourd’hui trois modèles d’horloges épigénétiques, à savoir les horloges de Hannum, de Weidner et de Horvath. Ces horloges diffèrent essentiellement par les sites CpG associés à l’âge utilisés pour construire ces biomarqueurs. En effet, James Horvath utilise un ensemble de 353 sites CpG pour son horloge, tandis que Gregory Hannum utilise un ensemble de 71 sites et Carola Ingrid Weidner en utilise 3 [5]. A noter que pour que l’estimation de l’âge chronologique soit la plus juste possible, il est préférable d’avoir un grand ensemble de dinucléotides CpG. Plus les ensembles sont grands et plus les estimateurs sont justes et robustes. Les horloges de Horvath et de Hannum sont donc actuellement les meilleurs estimateurs [2]. Ces deux horloges épigénétiques montrent une grande corrélation entre l’âge prédit et l’âge chronologique, avec un écart moyen de 3,6 ans pour celle d’Horvath et de 4,9 ans pour celle de Hannum [2].
Les horloges épigénétiques de Horvath et Hannum sont, de plus, capables de prédire la mortalité indépendamment des facteurs à risques classiques tels que l’âge, le poids, le tabagisme et l’alcoolisme, entre autres [2], en se basant uniquement sur les profils de méthylation des sites CpG associés à l’âge.
Dans sa dernière publication [1], Steve Horvath fait état de son horloge épigénétique comme étant la plus puissante actuellement disponible. En plus d’estimer l’âge chronologique avec une grande justesse, l’horloge épigénétique de Horvath est aussi la seule à pouvoir s’appliquer à plusieurs tissus. En effet, elle est la première qui mesure précisément l’âge épigénétique de nos cellules, de nos tissus et/ou de nos organes, et ce de manière distincte et spécifique [1,3]. Cette spécificité est l’une des caractéristiques les plus importantes de l’horloge épigénétique d’Horvath, et fait d’elle l’estimateur le plus utilisé dans la recherche contre le vieillissement [1]. En plus de cela, l’horloge de Horvath propose un panel de 353 sites CpG dont les profils de méthylations ont été identifiés et classés: 193 sites CpG hyperméthylés et 160 sites CpG hypométhylés avec l’âge.
L’horloge épigénétique et les pathologies liées à l’âge
Les maladies du vieillissement naissent toutes d’un dérèglement cellulaire ayant lieu à un moment ou à un autre au cours de notre vie. Ces dérèglements ont tendance à s’accélérer avec l’âge et à accroître notre âge biologique, qui va différer de plus en plus de notre âge chronologique : c’est l’accélération du vieillissement. Ce processus traduit un vieillissement prématuré du tissu en question et est associé à de nombreuses pathologies liées à l’âge. En effet, l’accélération du vieillissement est associée à un risque élevé de développer certains cancers et à la mortalité liée à ces cancers [6]. Dans le même sens, tous les tissus cancéreux montrent des signes d’accélération du vieillissement [3]. L’accélération du vieillissement est aussi associée à des pathologies telles que les maladies cardiovasculaires [6], la maladie de Parkinson et le syndrome de Werner, une maladie montrant un phénotype de vieillissement accéléré. Enfin, le syndrome de Down (trisomie 21) est associé à une accélération de l’âge épigénétique dans le sang et le cerveau [3]. Comme l’horloge épigénétique s’applique à beaucoup de tissus, elle permet de comparer les différences d’âges biologiques entre les organes d’un même individu, et de détecter ainsi un tissu qui montre une accélération du vieillissement, sous-entendant le développement d’une pathologie [3].

L’horloge épigénétique est un estimateur de l’âge biologique et un biomarqueur du vieillissement. Sa robustesse et son application à différentes sources d’ADN fait d’elle le meilleur estimateur actuellement disponible. L’âge prédit par la méthylation de l’ADN permet d’étudier le développement humain, le vieillissement et les pathologies liées à l’âge. Il peut aussi devenir un bon outil pour évaluer les thérapies anti-vieillissement [3]. A plus long terme, le but de ce biomarqueur du vieillissement sera l’identification et la validation des interventions épigénétiques anti-âge sur l’Homme.
Tout notre dossier sur l’épigénétique du vieillissement et la longévité :
Les altérations épigénétiques comme causes du vieillissement
Comprendre les altérations épigénétiques qui entraînent le vieillissement : récapitulatif des mécanismes impliqués.
Partie 2 : Épigénétique et ARNs non codants : le rôle des microARN et LncARN sur la longévité
La totalité de l’ADN ne code pas forcément des protéines ; les ARN non-codants tels que les microARN jouent aussi un rôle dans le processus de vieillissement.
Partie 4 : Epigenome editing, une technologie anti-vieillissement et pro-longévité
 Avec la naissance de l’épigénétique, une nouvelle technologie a vu le jour : l’epigenome editing, grâce à des avancées telles que l’outil CRISPR-Cas9.
Avec la naissance de l’épigénétique, une nouvelle technologie a vu le jour : l’epigenome editing, grâce à des avancées telles que l’outil CRISPR-Cas9.
Partie 1 : Les mécanismes moléculaires des altérations épigénétiques dans le vieillissement
Qu’est-ce que l’épigénétique ? Comment les altérations moléculaires entraînant le vieillissement en arrivent-elles à se produire ?
Partie 3 : L’horloge épigénétique, puissant outil de mesure du vieillissement
 On peut utiliser l’épigénétique comme un outil de mesure du vieillissement, en cartographiant les modifications qui surviennent avec l’âge.
On peut utiliser l’épigénétique comme un outil de mesure du vieillissement, en cartographiant les modifications qui surviennent avec l’âge.
Références :
[1] Steve Horvath and Kenneth Raj. DNA methylation-based biomarkers and the epigenetic clock theory of ageing. Nature Reviews | Genetics (April 2018)
[2] Jylhävä J., Pedersen N. L. & Hägg S. Biological age predictors. EBioMedicine 21, 29–36 (2017).
[3] Horvath Genome Biology, 14:R115 http://genomebiology.com//14/10/R115
[4] Perna et al. Clinical Epigenetics (2016) 8:64 DOI 10.1186/s13148-016-0228-z
[5] Weidner et al. Genome Biology 2014, 15:R24 http://genomebiology.com/2014/15/2/R24
[6] Declerck, K., Mechanisms of Ageing and Development (2018), https://doi.org/10.1016/j.mad.2018.01.002
Anne Fischer

Author
Auteur
Anne is studying medicine science at the Institute of Pharmaceutical and Biological Science in Lyon and she has graduated with a Bachelor’s degree in molecular and cellular biology at the University of Strasbourg.
More about the Long Long Life team
Anne étudie les sciences du médicament à l’Institut des Sciences Pharmaceutiques et Biologiques de Lyon. Elle est titulaire d’une licence en biologie moléculaire et cellulaire de l’Université de Strasbourg.
En savoir plus sur l’équipe de Long Long Life
Dr Guilhem Velvé Casquillas

Author/Reviewer
Auteur/Relecteur
Physics PhD, CEO NBIC Valley, CEO Long Long Life, CEO Elvesys Microfluidic Innovation Center
More about the Long Long Life team
Docteur en physique, CEO NBIC Valley, CEO Long Long Life, CEO Elvesys Microfluidic Innovation Center
En savoir plus sur l’équipe de Long Long Life