Epigenome editing, une technologie pour la longévité
L’épigénétique regroupe tous les mécanismes qui régulent l’expression des gènes, à savoir la méthylation de l’ADN, les modifications d’histones et le remodelage chromatinien. Ces mécanismes sont introduits sur le génome par des enzymes et des ARN non codants. Avec l’âge, des erreurs épigénétiques se produisent, causant de nombreuses pathologies comme les cancers [1]. Cependant, les modifications épigénétiques sont réversibles et il est possible de cibler leurs origines pour les renverser. Manipuler ces erreurs permet de comprendre leur rôle dans le vieillissement et le développement de pathologies, mais aussi de développer des nouvelles thérapies. Récemment, la technologie d’ “epigenome editing”, comprenez littéralement “une technologie d’édition du génome”, a été développée, dont les outils ciblent les enzymes et les ARN non-codants responsables des modifications, permettant ainsi de manipuler l’épigénome [2].
Epigenome Editing : qu’est-ce que c’est ?

Dans le terme anglais “epigenome editing”, l’épigénome fait référence à l’état épigénétique d’une cellule, tandis que le terme “editing” traduit la manipulation de cet état pour modifier les marques épigénétiques présentes. L’édition épigénétique est donc une technologie de révision de l’état épigénétique du génome [1], modifiant ainsi le profil d’expression des gènes d’une cellule. Elle est actuellement l’unique technologie qui permet de moduler l’épigénome [1].
Les outils utilisés pour modifier les marques épigénétiques sont des protéines chimères, composées de deux parties : un domaine de liaison à l’ADN, permettant, comme son nom l’indique, aux protéines de s’associer à l’ADN, et un domaine comprenant un facteur épigénétique (enzyme ou autre) qui va pouvoir modifier l’ADN [1]. Les domaines de liaison à l’ADN sont de trois différents types : les protéines en doigts de zinc (ou ZFP pour Zinc Finger Protein), les effecteurs TALE (Transcription Activator-Like Effectors) et le système CRISPR-Cas9 [2]. Ces protéines chimères sont des outils puissants pour créer des cellules isogéniques (des “clones”) et des animaux transgéniques (qui expriment ou non un gène spécifique) [3] faisant de l’édition épigénétique un outil puissant pour la recherche, la biotechnologie et la médecine.
Réviser les modifications épigénétiques, qui peuvent être à l’origine de pathologies liées à l’âge, offre un grand potentiel de développement thérapeutique contre ces maladies. L’édition épigénétique est une technologie qui s’applique très bien pour la recherche anti-âge [3]. Elle permet d’introduire des variations épigénétiques in vitro ou in vivo, utiles pour comprendre et expliquer le développement de pathologies, la sévérité de certains symptômes et le rôle de l’environnement. Cette approche complète les connaissances sur le développement de pathologies qu’une approche uniquement basée sur l’étude de la séquence d’ADN ne permet pas d’expliquer [3]. L’ “epigenome editing” peut induire une marque épigénétique, mais elle peut aussi l’enlever, comme c’est le cas par exemple, pour l’étude des cancers. En effet, des cellules cancéreuses peuvent être induites in vitro en introduisant des erreurs épigénétiques dans l’ADN de cellules normales, puis ces erreurs peuvent être supprimées des cellules cancéreuses [1].
Que ciblent les outils de l’ “epigenome editing” ?
Cette technologie cible donc les effecteurs moléculaires à l’origine de marques épigénétiques. L’action se fait par l’inhibition des enzymes qui apportent ou suppriment les modifications épigénétiques, ou en empêchant la liaison des ARN non-codants avec leurs cibles. Les ADN méthyltransférases (DNMT) sont les enzymes responsables de l’établissement et du maintien de la méthylation de l’ADN, et l’une des principales cibles de l’édition épigénétique. Les inhibiteurs des DNMT sont d’ailleurs les plus avancés dans les applications cliniques de l’”epigenome editing” [4]. Parallèlement, il existe actuellement au moins 232 enzymes capables de moduler les modifications post-traductionnelles des histones, et des thérapies épigénétiques basées sur les HDAC (Histone deacetylase : une enzyme qui permet de supprimer l’acétylation des histones) sont déjà en phase clinique [5]. En ciblant les enzymes responsables des marques épigénétiques, l’ ”epigenome editing” permet de cibler différents types de mutations épigénétiques telles que les mutations perte de fonction (où un gène n’est plus exprimé) et les mutations gain de fonction (où un gène est trop exprimé) [6].
Epigenome editing : Altérations épigénétiques et épi-médicaments
Les altérations épigénétiques sont l’une des causes majeures du vieillissement et de nombreuses pathologies [7]. C’est notamment le cas pour les cancers, dont la malignité vient souvent d’erreurs épigénétiques entraînant l’expression de gènes pro-cancer, appelés oncogènes. L’épigénétique du cancer est un des sujets de recherche les plus importants dans ce domaine et les mécanismes de cancérogenèse sont aujourd’hui de mieux en mieux compris et maîtrisés. Il est maintenant possible d’induire ou de supprimer un cancer par édition épigénétique dans des modèles cellulaires et animaux, avec l’espoir de transférer cela chez l’Homme dans les prochaines années. Un exemple de ces mécanismes est l’enzyme G9a, une méthylase qui va modifier une histone spécifique, et, suivant l’état de méthylation de cette histone, va pouvoir soit induire, soit supprimer un cancer dans un modèle in vitro [1]. On peut également citer la DNMT3A, un méthyltransférase responsable de la modification de l’ADN sur un gène particulier, appelé SOX2, et dont l’absence d’expression (pas de production de protéine à partir du gène), va entraîner une suppression de la croissance tumorale.

Les épi-médicaments (ou médicaments épigénétiques) se basent sur ces mécanismes, parfois bénéfiques, parfois délétères, pour les modifier dans le bon sens. Ce sont des composés capables de cibler les enzymes épigénétiques pour corriger les marques établies sur le génome. L’intérêt pour ces modulateurs épigénétiques est grandissant, notamment dans le traitement des cancers. En 2016, six épi-médicaments avaient reçu l’autorisation de la FDA (Food and Drug Administration) [8]. Par ailleurs d’autres médicaments sont en développement clinique, dont des inhibiteurs de méthylation de l’ADN et des inhibiteurs des enzymes histone déacétylases (HDAC), dont la surexpression est une caractéristique commune des pathologies humaines. Inhiber les HDAC permettrait de remédier à certaines caractéristiques des cancers comme la prolifération cellulaire, l’angiogenèse et la différenciation cellulaire [4]. Dernièrement, ce sont les inhibiteurs des histones acétyltransférases (HATi), des enzymes à l’origine de l’acétylation post-traductionnelle des histones, qui ont gagné de l’intérêt grâce à des résultats prometteurs sur des tumeurs solides. La cancérologie n’est pas le seul domaine pouvant tirer bénéfice de la technologie d’“epigenome editing” : l’administration d’un inhibiteur non spécifique des HDAC, la trichostatine, a par exemple permis de renverser des perturbations neuro-développementales chez des rats adultes [9].
Enfin, Il existe une classe de composés capables d’empêcher la liaison des ARN non-codants à leurs cibles : les antagomirs. Ils sont utilisé pour inhiber l’action des ARN non-codants en épigénétique. Il a été montré qu’un traitement avec l’antagomir du microARN 181a suite à un AVC réduisait la taille de l’infarctus, les déficits neuronaux, l’inflammation et apporté des effets neuroprotecteurs chez la souris [10]. Par ailleurs, l’étude a démontré que réduire le microARN 181a avant l’AVC protégeait les cellules du cerveau des lésions ischémiques in vivo et in vitro [10]. Toutefois, les épi-médicaments et les antagomirs sont des composés non spécifiques, pouvant atteindre tout type de tissu et d’organe. Cette caractéristique souligne les risques d’effets indésirables plus ou moins graves qui peuvent être observés avec de tels traitements.
L’ “epigenome editing” est une technologie novatrice dont les outils puissants ont révolutionné la recherche biomédicale. Elle offre des opportunités sans précédent pour étudier l’épigénétique du vieillissement et développer des thérapies contre les pathologies associées. Bien que des percées méthodologiques et conceptuelles soient encore nécessaires pour appliquer l’ “epigenome editing” en routine et dans un cadre clinique, un grand nombre de publications ont d’ores et déjà démontré le grand potentiel de cette technologie.
Tout notre dossier sur l’épigénétique du vieillissement et la longévité :
Les altérations épigénétiques comme causes du vieillissement
Comprendre les altérations épigénétiques qui entraînent le vieillissement : récapitulatif des mécanismes impliqués.
Partie 2 : Épigénétique et ARNs non codants : le rôle des microARN et LncARN sur la longévité
La totalité de l’ADN ne code pas forcément des protéines ; les ARN non-codants tels que les microARN jouent aussi un rôle dans le processus de vieillissement.
Partie 4 : Epigenome editing, une technologie anti-vieillissement et pro-longévité
 Avec la naissance de l’épigénétique, une nouvelle technologie a vu le jour : l’epigenome editing, grâce à des avancées telles que l’outil CRISPR-Cas9.
Avec la naissance de l’épigénétique, une nouvelle technologie a vu le jour : l’epigenome editing, grâce à des avancées telles que l’outil CRISPR-Cas9.
Partie 1 : Les mécanismes moléculaires des altérations épigénétiques dans le vieillissement
Qu’est-ce que l’épigénétique ? Comment les altérations moléculaires entraînant le vieillissement en arrivent-elles à se produire ?
Partie 3 : L’horloge épigénétique, puissant outil de mesure du vieillissement
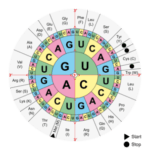 On peut utiliser l’épigénétique comme un outil de mesure du vieillissement, en cartographiant les modifications qui surviennent avec l’âge.
On peut utiliser l’épigénétique comme un outil de mesure du vieillissement, en cartographiant les modifications qui surviennent avec l’âge.
Références :
[1] Shota Nakade, Takashi Yamamoto, Tetsushi Sakuma, Cancer induction and suppression with transcriptional control and epigenome editing technologies, Journal of Human Genetics (2018) 63:187–194. https://doi.org/10.1038/s10038-017-0377-8
[2] Pratiksha I. Thakore, Joshua B. Black, Isaac B. Hilton and Charles A. Gersbach. Editing the Epigenome: Technologies for Programmable Transcriptional Modulation and Epigenetic Regulation, Nat Methods. 2016 February ; 13(2): 127–137. doi:10.1038/nmeth.3733.
[3] Cia-Hin Lau and Yousin Suh. Genome and Epigenome Editing in Mechanistic Studies of Human Aging and Aging-Related Disease, Gerontology. 2017 ; 63(2): 103–117. doi:10.1159/000452972.
[4] Graça et al. Clinical Epigenetics (2016) 8:98. DOI 10.1186/s13148-016-0264-8
[5] Tim J. Wigle, Promoting Illiteracy in Epigenetics: An Emerging Therapeutic Strategy, Current Chemical Genomics, 2011, 5, (Suppl 1-M1) 48-5.
[6] Sophia Xiao Pfister and Alan Ashworth. Marked for death: targeting epigenetic changes in cancer, Nature Reviews, Drug Discovery, Volume 16 (April 2017), 241-263.
[7] Carlos Lopez-Otin, Maria A. Blasco, Linda Partridge, Manuel Serrano and Guido Kroemer. The Hallmarks of Aging, Cell 153, June 2013, 1194-1217.
[8] Alfonso Dueñas-González, J. Jesús Naveja, José L. Medina-Franco, Introduction of Epigenetic Targets in Drug Discovery and Current Status of Epi-Drugs and Epi-Probes, Epi-Informatics. http://dx.doi.org/10.1016/B978-0-12-802808-7.00001-0
[9] Moshe Szyf. Prospects for the development of epigenetic drugs for CNS conditions, Nature Reviews, Drug Discovery Volume 14 (July 2015), 461-474.
[10] Li-Jun Xu, Yi-Bing Ouyang, Xiaoxing Xiong, Creed M Stary, and Rona G Giffard. Post-stroke treatment with miR-181 antagomir reduces injury and improves long-term behavioral recovery in mice after focal cerebral ischemia. Exp Neurol. 2015 February ; 264: 1–7. doi:10.1016/j.expneurol.2014.11.007.
Anne Fischer

Author
Auteur
Anne is studying medicine science at the Institute of Pharmaceutical and Biological Science in Lyon and she has graduated with a Bachelor’s degree in molecular and cellular biology at the University of Strasbourg.
More about the Long Long Life team
Anne étudie les sciences du médicament à l’Institut des Sciences Pharmaceutiques et Biologiques de Lyon. Elle est titulaire d’une licence en biologie moléculaire et cellulaire de l’Université de Strasbourg.
En savoir plus sur l’équipe de Long Long Life
Dr Guilhem Velvé Casquillas

Author/Reviewer
Auteur/Relecteur
Physics PhD, CEO NBIC Valley, CEO Long Long Life, CEO Elvesys Microfluidic Innovation Center
More about the Long Long Life team
Docteur en physique, CEO NBIC Valley, CEO Long Long Life, CEO Elvesys Microfluidic Innovation Center
En savoir plus sur l’équipe de Long Long Life