Mesure du vieillissement: Les télomères des témoins de l’âge physiologique
La mesure de la longueur des télomères est un outil très précis pour déterminer l’âge physiologique de nos cellules et de nos organes.
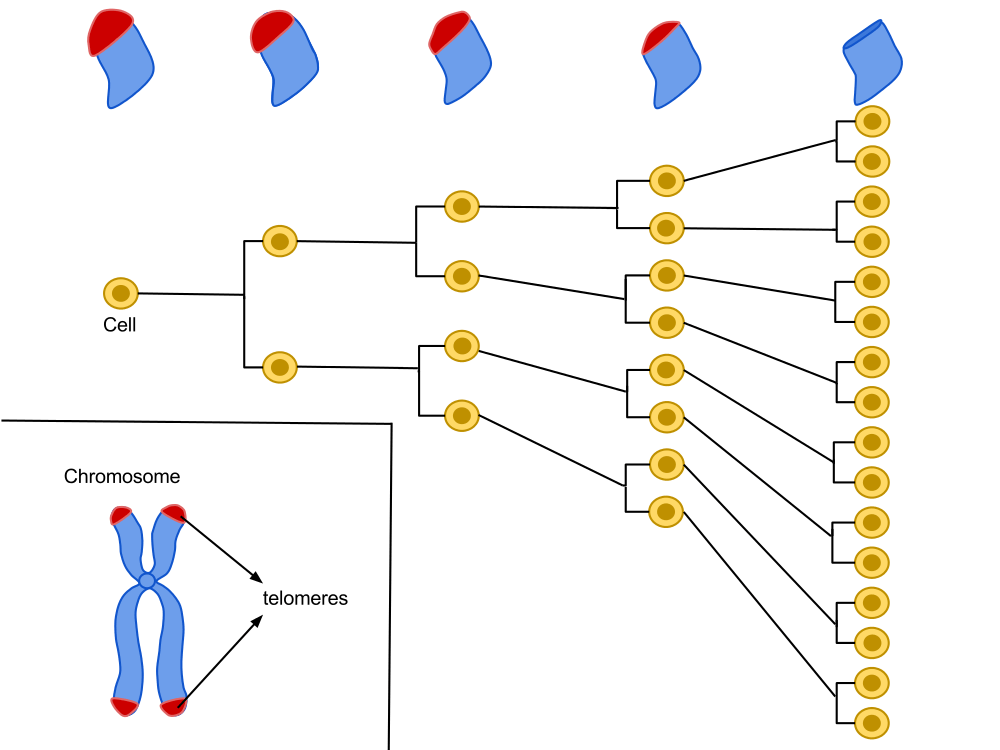
Situées aux extrémités de nos chromosomes, les télomères sont des séquences très répétitives comportant la suite de nucléotides TTAGGG. Une cellule est programmée pour se diviser un certain nombre de fois et, à chaque division cellulaire, ces extrémités chromosomiques se raccourcissent un peu plus, jusqu’à atteindre une taille critique. La cellule va alors stopper sa croissance pour entrer en sénescence.
Le mode de vie, les habitudes alimentaires le stress, les facteurs environnementaux ainsi que l’âge peuvent accélérer le raccourcissement des télomères. La mesure de leur longueur peut donc fournir des indications précieuses sur l’avancement de l’âge réel de nos cellules, ainsi que sur les facteurs l’influençant. Pour toutes ces raisons, la mesure des télomères est un remarquable moyen métrologique du degré de vieillissement d’un organisme, et elle peut inciter les individus à prendre des mesures afin de préserver leur santé.
Les travaux de Hayflick ont montré qu’il existe un capital de divisions pour plusieurs lignées cellulaires. Il est proportionnel à la longévité de l’espèce et connaît des écarts entre les individus d’une même espèce. A chaque cycle de division cellulaire, l’extrémité des chromosomes (télomère) perd un fragment d’ADN. Après plusieurs divisions, la fonction du télomère, qui contribue à maintenir la stabilité de l’ADN, est altérée, ce qui pourrait être le substratum de «l’horloge biologique».
L’échantillon à tester : la mesure de la longueur des télomères peut être faite sur des échantillons cellulaires ou tissulaires, cependant on privilégiera d’effectuer cette mesure sur les télomères des leucocytes, un type de cellules présentes dans le sang, permettant un prélèvement peu invasif.
Cinq grandes méthodes de mesure des télomères pour la métrologie du vieillissement
Southern blots of Terminal Restriction Fragments (TRFs)
Développée en 1990, il s’agit de la technique la plus archaïque, mais aussi de la plus largement utilisée. Cette technique estime le nombre moyen de répétitions terminales TTAGGG portées par l’ensemble des chromosomes. Elle repose sur la technique d’hybridation in situ qui identifie les répétitions TTAGGG coiffant les télomères. L’ADN télomérique est digéré par des enzymes de restriction, il en résulte plusieurs petits fragments d’ADN de tailles différentes. Afin de connaître la taille de chaque fragment d’ADN télomérique, on utilise le Southern Blot.
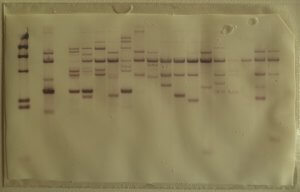
Pour ce faire, les fragments télomériques obtenus après digestion sont séparés par électrophorèse sur gel puis transférés sur une membrane de nitrocellulose ou de nylon, supports solides qui facilitent la dénaturation de l’ADN (passage de la forme double-brin à simple-brin) et son hybridation avec une sonde. Cette étape est cruciale afin de permettre l’hybridation d’une sonde radioactive (fragment d’ADN complémentaire de la séquence recherchée). La position des fragments de restriction est alors révélée par radiographie et leur taille est estimée par comparaison entre la distance qu’ils ont parcourue dans le gel et celle couverte par des fragments de longueur connue [1][2].
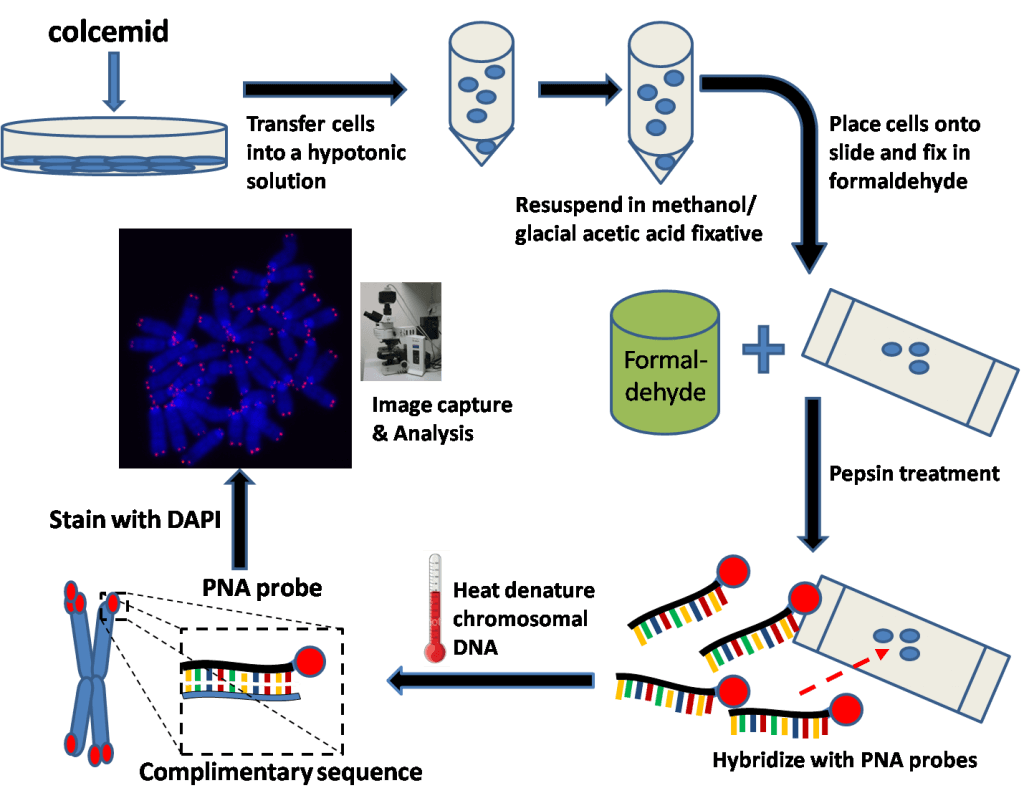
Q-Fish
Il s’agit aussi d’une hybridation in situ, mais contrairement au Southern Blot, la sonde n’est pas radioactive, mais fluorescente. L’inconvénient de cette méthode, c’est qu’elle requiert une importante quantité́ d’ADN pouvant aller jusqu’à 20 μg, alors que quelques ng suffisent pour d’autres techniques comme la PCR-Q [3][4].
Flow-FISH
La technique de Flow-FISH est similaire au Q-FISH à l’exception du fait qu’elle permet une analyse directe des télomères sans extraction de l’ADN au préalable. Par la suite, les cellules marquées sont triées dans un cytomètre en flux. Cette méthode est fort coûteuse et peu utilisée, car elle nécessite d’importants équipements. Néanmoins, elle reste très intéressante: elle permet de réduire les étapes de purification et permet l’analyse simultanée de la longueur de télomère dans différents type cellulaire [7][8].
TAT pour la mesure de la longueur des télomères
TAT® évalue la longueur des télomères individuellement. La technologie TAT® est basée sur l’hybridation fluorescente in situ à haut débit, permise par une approche High Content Screening (HCS). TAT® fournit une mesure complète de la longueur des télomères par l’intermédiaire d’un histogramme. Il donne des indications sur les télomères des plus courts aux plus longs, donne la fréquence par classe de longueur, la moyenne ainsi que les valeurs médianes [9].
PCR-Q
Mise au point en 2003, la PCR-Q est une technique plus rapide et plus aisée. Cette technique est basée sur le principe de l’hybridation. Une séquence d’ADN est extraite puis placée dans une machine qui va permettre d’effectuer trois étapes différentes (répétées une quarantaine de fois): une dénaturation (passage de l’ADN double brin à simple brin), une hybridation avec la sonde puis une amplification du produit hybridé. La sonde est un fragment d’ADN complémentaire de la séquence d’intérêt et va permettre d’amplifier, c’est à dire d’augmenter le nombre de copies, de ce gène. Plus une séquence d’ADN est amplifiée rapidement, plus il est présent dans un échantillon donné.
Grâce à plusieurs paramètres, notamment le ratio du nombre de copies du motif télomérique (T) par rapport à un gène contrôle (S) (T/S), on peut déterminer le nombre de répétitions TTAGGG, caractéristiques de l’ADN télomérique [2][5][6].
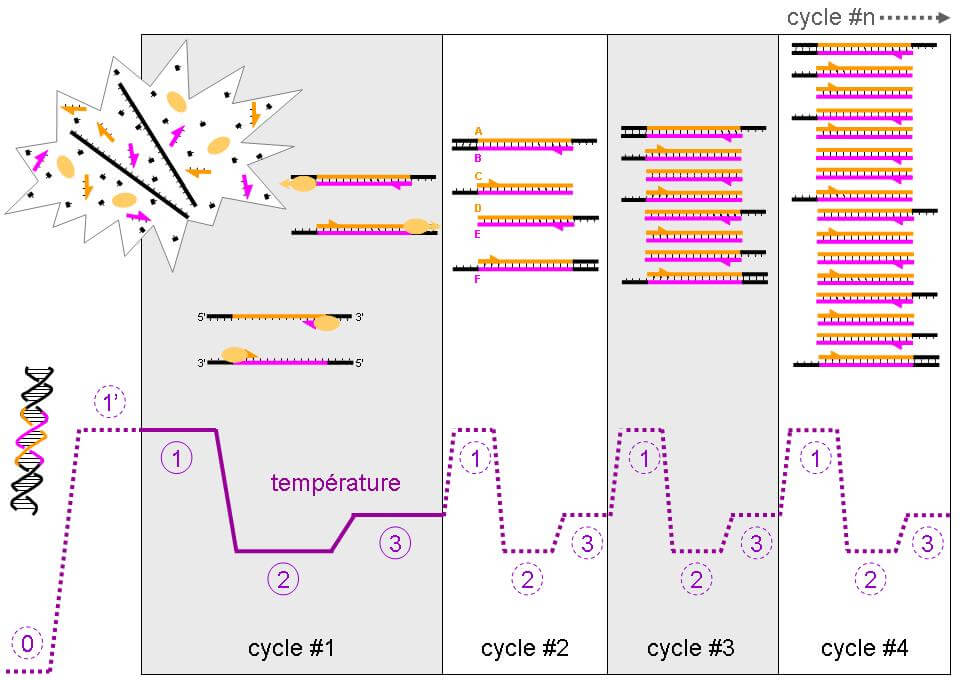
STELA (Single TElomere Length Analysis)
Cette technique diffère de la PCR-Q par le fait qu’elle permet d’amplifier, non pas un fragment de télomère mais la totalité de sa séquence. Son principe est le même pour le reste de la procédure. Elle est en revanche plus longue car elle nécessite une analyse chromosome par chromosome et non pas sur de l’ADN total [2][7][8].
La mesure de la longueur des télomères et métrologie du vieillissement
Les techniques de PCR semblent être les meilleures en terme de reproductibilité, mais à l’instar des méthodes basées sur l’hybridation in situ, elles ne peuvent amplifier des télomères de plus de 25 kb. Il est possible d’observer des télomères de plus de 50 kb, mais on préfèrera dans ce cas le Southern Blot.
On sait que tous les organes du corps ne vieillissent pas de la même façon, et même si les leucocytes sont un type cellulaire représentatif pour l’étude du vieillissement, les tests ci-contre analysent essentiellement des populations cellulaires provenant d’un échantillon sanguin, et cela reste encore trop réducteur. L’analyse de la longueur télomérique faite à partir d’un prélèvement tissulaire (biopsie) est possible, mais requiert un encadrement médical et une intervention très invasive.
Où peut-on demander une analyse de nos télomères ?
Un nombre florissant de laboratoires se sont lancés sur ce marché, chacun commercialisant sa propre version de kits d’analyse de longueur des télomères. La société Life Length se place comme le leader du domaine et possède de nombreux laboratoires partenaires qui proposent l’envoie d’échantillon par la Poste comme Les Laboratoires Réunis ou bien une analyse sur place comme La Clinique Crillon.
Cette technique d’avenir est encore balbutiante mais promet de belles envolées dans les années à venir tant grâce à l’avancée des méthodes disponibles qu’à la multiplication des laboratoires proposant leurs services, diminuant ainsi coût, temps et risques de ces analyses.
Tous les articles de notre dossier « Télomères et vieillissement » :
Les télomères : au cœur des processus de vieillissement
 Le raccourcissement des télomères est connu pour avoir une influence sur le vieillissement sans que cela ne soit pleinement explicité. Mais comment fonctionnent-ils ? Sur quels mécanismes biologiques agissent-ils ? Et pourquoi les qualifier d’ « horloges biologiques » de notre corps ?
Le raccourcissement des télomères est connu pour avoir une influence sur le vieillissement sans que cela ne soit pleinement explicité. Mais comment fonctionnent-ils ? Sur quels mécanismes biologiques agissent-ils ? Et pourquoi les qualifier d’ « horloges biologiques » de notre corps ?
Partie 1 : Causes et effets du raccourcissement des télomères au cours du vieillissement
 La vitesse de raccourcissement des télomères et le vieillissement varient d’un individu à l’autre, sans que cela ne soit encore pleinement clarifié. En effet, les causes qui pourraient expliquer les différences de longueur de télomères sont très variées.
La vitesse de raccourcissement des télomères et le vieillissement varient d’un individu à l’autre, sans que cela ne soit encore pleinement clarifié. En effet, les causes qui pourraient expliquer les différences de longueur de télomères sont très variées.
Partie 2 : L’influence de la télomérase sur les télomères et le vieillissement
 La longueur des télomères et la télomérase semblent être des facteurs clés du processus de vieillissement. De nombreuses études sur les maladies dues à des mutations des composants de la télomérase ont démontré que cela entraîne un mauvais renouvellement des cellules, soit l’un des phénotypes liés à l’âge.
La longueur des télomères et la télomérase semblent être des facteurs clés du processus de vieillissement. De nombreuses études sur les maladies dues à des mutations des composants de la télomérase ont démontré que cela entraîne un mauvais renouvellement des cellules, soit l’un des phénotypes liés à l’âge.
 L’expression de la télomérase est diminuée quelques semaines après la naissance dans la majorité des tissus adultes, à l’exception de certains types cellulaires, telles que les cellules souches. On peut alors se demander s’il existe un lien entre la diminution du stock de cellules souches avec l’âge, le fonctionnement de la télomérase et la longueur des télomères.
L’expression de la télomérase est diminuée quelques semaines après la naissance dans la majorité des tissus adultes, à l’exception de certains types cellulaires, telles que les cellules souches. On peut alors se demander s’il existe un lien entre la diminution du stock de cellules souches avec l’âge, le fonctionnement de la télomérase et la longueur des télomères.
Partie 4 : Vers une métrologie du vieillissement à partir du télomère
 Des méthodes de métrologie du vieillissement se basant sur la longueur des télomères ont été développée. Aujourd’hui, on en dénombre 5 principales, dont TAT ou STELA. Elles permettent toutes, à partir de la longueur des télomères, de fournir des indications précieuses sur l’avancement de l’âge physiologique ainsi que sur le vieillissement.
Des méthodes de métrologie du vieillissement se basant sur la longueur des télomères ont été développée. Aujourd’hui, on en dénombre 5 principales, dont TAT ou STELA. Elles permettent toutes, à partir de la longueur des télomères, de fournir des indications précieuses sur l’avancement de l’âge physiologique ainsi que sur le vieillissement.
Partie 5 : Télomères, vieillissement et thérapies
 La longueur des télomères constitue une piste intéressante pour élaborer des thérapies afin de lutter contre le vieillissement. On peut citer l’exemple d’Elizabeth Parrish, PDG de Bioviva ; elle a testé sur elle-même une thérapie génique développée par son propre laboratoire, thérapie qui vise à rallonger de ses télomères afin de « rajeunir » !
La longueur des télomères constitue une piste intéressante pour élaborer des thérapies afin de lutter contre le vieillissement. On peut citer l’exemple d’Elizabeth Parrish, PDG de Bioviva ; elle a testé sur elle-même une thérapie génique développée par son propre laboratoire, thérapie qui vise à rallonger de ses télomères afin de « rajeunir » !
Farah Bahou

Author
Auteure
Farah studied biochemistry, therapeutics and molecular and biopharmaceutical innovation at Aix-Marseille university and Paris 7 Diderot university.
More about the Long Long Life team
Farah a étudié la biochimie, la thérapeutique et les innovations moléculaires et biopharmaceutiques à l’université d’Aix-Marseille et à l’université Paris 7 Diderot.
En savoir plus sur l’équipe de Long Long Life
Dr Guilhem Velvé Casquillas

Author/Reviewer
Auteur/Relecteur
Physics PhD, CEO NBIC Valley, CEO Long Long Life, CEO Elvesys Microfluidic Innovation Center
More about the Long Long Life team
Docteur en physique, CEO NBIC Valley, CEO Long Long Life, CEO Elvesys Microfluidic Innovation Center
En savoir plus sur l’équipe de Long Long Life
Références
[1] Kimura, M., Stone, R. C., et al. Measurement of telomere length by the Southern blot analysis of terminal restriction fragment lengths. Nature protocols, 2010, 5(9), 1596-1607.
[2] Martin-Ruiz, C. M., Baird, D., et al. Reproducibility of telomere length assessment: an international collaborative study. International journal of epidemiology, 2014, dyu191.
[3] Cawthon, R. M., Smith, K. R., O’Brien, E., Sivatchenko, A., & Kerber, R. A. Association between telomere length in blood and mortality in people aged 60 years or older. The Lancet, 2003, 361(9355), 393-395.
[4] Lansdorp, P. M., Verwoerd, N. P., et al. Heterogeneity in telomere length of human chromosomes. Human molecular genetics, 1996, 5(5), 685-691.
[5] Gutierrez-Rodrigues, F., Santana-Lemos, B. A., Scheucher, P. S., Alves-Paiva, R. M., & Calado, R. T. Direct comparison of flow-FISH and qPCR as diagnostic tests for telomere length measurement in humans. PLoS One, 2014, 9(11), e113747.
[6] Aviv, A., Hunt, S. C., Lin, J., Cao, X., Kimura, M., & Blackburn, E. Impartial comparative analysis of measurement of leukocyte telomere length/DNA content by Southern blots and qPCR. Nucleic acids research, 2011, gkr634.
[9] Bendix, L., Horn, P. B., Jensen, U. B., Rubelj, I., & Kolvraa, S. The load of short telomeres, estimated by a new method, Universal STELA, correlates with number of senescent cells. Aging cell, 2010, 9(3), 383-397.
[8] Letsolo, B. T., Rowson, J., & Baird, D. M. Fusion of short telomeres in human cells is characterized by extensive deletion and microhomology, and can result in complex rearrangements. Nucleic acids research, 2010, 38(6), 1841-1852.
[9] Baerlocher, G. M., Vulto, I., De Jong, G., & Lansdorp, P. M. Flow cytometry and FISH to measure the average length of telomeres (flow FISH). Nature protocols, 2006, 1(5), 2365-2376.