La génomique, on le rappelle, c’est l’étude du génome, c’est à dire, la totalité de notre ADN. Quand on sait que si l’on dépliait la totalité de l’ADN contenu dans notre corps, on pourrait couvrir 1000 fois la distance de la Terre au Soleil, on se demande parfois comment il est possible d’analyser une telle quantité de données !
Comment analyse-t-on un génome ?

En 1953, Watson & Crick, deux chercheurs se basant sur les données crystallographiques de Wilkins & Franklin, ont réussi à élucider la structure de l’ADN, ouvrant un tout nouveau champ d’étude, notamment concernant les processus de réplication et de transcription de l’ADN. Le séquençage était encore loin mais l’idée a germé chez les chercheurs et en 1965, le premier transcriptome a été séquencé, celui d’une levure, Saccharomyces cerevisiae [1]. Cependant, l’ARN c’est bien, l’ADN c’est mieux ! Les avancées technologiques ont permis de développer différentes techniques de séquençage, qui ont valu un prix Nobel de chimie à Gilbert & Sanger en 1970. Enfin, en 1977, le premier génome à être entièrement séquencé appartenait à un virus bactériophage [2].
En quoi consiste le séquençage ?
Séquençage par la méthode de Sanger [3] – par synthèse enzymatique
C’est la technique la plus utilisée actuellement et de nombreuses améliorations lui ont été apportées depuis les années 70. Le principe est relativement simple et basé sur le même mécanisme que la réplication naturelle de l’ADN : une amorce (une petite séquence d’ADN) va initier la synthèse d’un brin d’ADN complémentaire à celui que l’ont veut séquencer, une ADN polymérase va procéder à l’élongation de ce brin, puis un mélange de désoxyribonucléotides (dATP, dCTP, dGTP et dTTP) et de di-désoxyribonucléotides (ddATP, ddCTP, ddGTP ou ddTTP) va être introduit dans le mélange. Les désoxyribonucléotides vont être intégrés normalement et participer à la synthèse du brin d’ADN (et donner l’adénine, la cytosine, la guanine et la thymine, les quatre bases de l’ADN). En revanche, les di-desoxyribonucléotides (des homologues des désoxyribonucléotides mais n’ayant pas le groupement chimique nécessaire à l’action de l’ADN-polymérase), vont s’intégrer au brin en cours de synthèse et provoquer sa cassure. Ainsi, si l’on a introduit du ddCTP au mélange, le brin en cours de synthèse va se couper à chaque cytosine. Pour un séquençage complet, il suffit de recommencer la manœuvre avec les trois di-désoxyribonucléotides restants. L’expérimentateur se retrouvera avec des fragments d’ADN de différentes longueurs pour lesquels il saura exactement à quel di-désoxyribonucléotide ils se sont cassés. Chaque fragment est analysé et remis dans l’ordre suivant son poids moléculaire, permettant de retrouver la séquence exacte de l’ADN.
Séquençage par la méthode de Gilbert [4] – par dégradation chimique
Contrairement à la méthode de Sanger, la méthode Gilbert repose sur une dégradation de l’ADN : le but est de réaliser des coupures sélectives grâce à des procédés chimiques brisant l’ADN en fragments, qui seront remis dans l’ordre par la suite. Une fois l’ADN d’intérêt marqué avec un traceur radioactif, il est dénaturé (double brin vers simple brin) et soumis à des modifications chimiques, mises au point par Gilbert lui-même, spécifiques de chaque base constituant l’ADN. A l’endroit de la modification, l’ADN est ensuite coupé puis chaque fragment est analysé et remis dans l’ordre suivant son poids moléculaire (comme pour la méthode de Sanger).
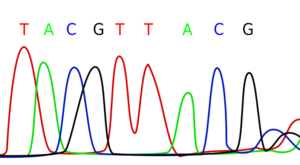
Comment séquencer un génome entier ?
Les deux techniques dont nous venons de parler ont été largement améliorées depuis leur découverte, notamment en terme de préparation des échantillons, de séparation et de détection des fragments d’ADN. Ces avancées ont permis d’automatiser le séquençage avec des machines de plus en plus performantes. Cependant, le génome entier fait plusieurs milliards de bases et aucune machine n’a aujourd’hui la capacité de traiter autant d’information. Il est nécessaire de préparer l’ADN, en le traitant avec des enzymes de restrictions ou des ultrasons, le but étant d’obtenir des fragments que l’on pourra séquencer. L’arrivée de la bio-informatique et des nanotechnologies a également révolutionné le domaine pour créer la génomique telle qu’on la connait actuellement.
HTS, NGS, microarray, GWAS… quésaco ?
Les dernières évolutions du séquençage ont donné naissance à beaucoup d’acronymes, pas toujours faciles à comprendre. HTS veut dire « High-Throughput Sequencing » soit « séquençage à haut débit ». Il est souvent associé aux NGS, « Next Generation Sequencing » ou « séquençage nouvelle génération », car les deux approches ont vu le jour au début des années 2000 et se recoupent [5]. Le but de ces techniques est d’augmenter le nombre de séquences décodées par série d’analyse, jusqu’à quelques millions de fragments d’ADN, tout en baissant le prix de ces tests. Elles ont bouleversé la génomique en rendant accessible, en terme de temps et de finances, des études jusque là complexes et couteuses. Elles permettent également, et c’est une révolution en soi, d’analyser une seule copie d’ADN, rendant ainsi possible des analyses sur de tous petits échantillons [5].
Le pyroséquençage, qui fait partie des HTS/NGS, est actuellement le plus utilisé : il se base sur la méthode de Sanger mais utilise des nucléotides pyrophosphatés à la place des di-desoxyribonucléotides. Lorsqu’ils sont incorporés dans le brin d’ADN en cours de synthèse, au lieu de stopper l’élongation, ils vont libérer un pyrophosphate qui va être transformé et émettre une lumière. On obtient au final un graphe avec des pics qui correspondent à l’incorporation des nucléotides marqués, et dont la hauteur reflète le nombre de nucléotides intégrés à la séquence d’ADN. Avec des outils bioinformatiques, il est ensuite possible de déterminer la séquence de l’ADN. L’intérêt majeur de cette technique est l’analyse en parallèle de plusieurs milliers de fragments, permettant d’obtenir des résultats en quelques heures [5].

Les puces à ADN, ou « DNA-microarray« , utilisent un tout autre mécanisme : des séquences connus d’ADN sont fixées sur une plaque (la puce) et l’ADN à tester est injecté sur cette surface. Lorsqu’il est complémentaire d’une séquence sur la puce, il s’hybride, émet une lumière détectable et on obtient un spectre d’hybridation qui peut nous donner plusieurs informations : niveau d’expression d’un gène donné, mutations, séquençage, interactions avec d’autres molécules… [6]
L’approche GWAS, « Genome-Wide Association Studies » ou « études d’associations pangénomique », est une technique de génétique croisée à la génomique. Comme son nom l’indique, elle étudie les mutations génétiques, non pas au niveau d’un gène mais en prenant en compte la totalité du génome. Ce n’est pas une technique de séquençage à proprement parler, mais elle permet d’identifier des mutations rapidement et avec fiabilité [7]. Elle met en évidence majoritairement ce qu’on appelle les SNP, « single nucleotide polymorphism », qui correspondent à des mutations ponctuelles d’une seule base au sein d’un séquence d’ADN complète. Elle met ensuite ces SNP en lien avec des maladies connues, permettant ainsi de faire le lien entre la survenue d’une mutation et une situation pathologique [7].
Plus récemment, les « single-cell genomics » ont fait leur apparition, avec comme ambition d’obtenir des informations sur l’ADN d’une seule cellule [8]. Contrairement aux autres techniques qui tirent leurs données de milliers de cellules, cette approche souhaite prendre en compte l’hétérogénéité des populations cellulaires et la diversité génomique existant entre les cellules d’un même organe.
La génomique appliquée aux pathologies du vieillissement
Nous avons parlé des différentes techniques d’analyse du génome, à présent que faire des données obtenues ? Le séquençage donne des milliers d’informations qu’il faut ensuite traiter. L’application évidente est la corrélation entre les modifications du génome et les maladies existantes, une approche similaire au GWAS. Grâce au séquençage, on peut également identifier des mutations apparaissant de novo, des mutations rares que d’autres techniques ne permettent pas de discerner ou mettre en évidence des variants de gènes, nous donnant de nouvelles perspectives thérapeutiques [6].
Génétique, génomique et épigénomique
La génétique diffère de la génomique par son approche plus ciblée, s’intéressant à un gène spécifique, à ses mutations possibles et à sa transmission. La génomique, on l’a vu, s’intéresse au génome entier et à ses variations. Ce type d’étude à donné naissance à de nouveaux domaines de recherche, dont le plus important est l’épigénomique : un mélange de génomique et d’épigénétique. Comme la génomique et la génétique, l’épigénomique diffère de l’épigénétique par son sujet d’étude, le génome, ou plus précisément l’épigénome, qui représente l’ensemble des modifications du matériel génétique d’une cellule (lien vers le dossier épigénétique).
En combinant ces approches, on obtient des cartes génomiques, indiquant les mutations, les polymorphismes, les variants génétiques ou encore le taux de méthylation de l’ADN [9].

Le Cancer
Plusieurs équipes dans le monde se sont intéressées à la comparaison du génome de cellules normales à celui de cellules cancéreuses, tout particulièrement en termes de variants structurels. Un variant structurel c’est un petit segment d’ADN dont la séquence reste la même mais qui change de conformation (inversion, translocation) donnant lieu à une diversité cellulaire, bénéfique uniquement jusqu’à un certain stade [10]. Ces variants sont impliqués dans beaucoup de maladies, lorsque leur taux augmente, mais restent très difficiles à détecter. Les techniques de génomique sont les seules à pouvoir les identifier et ce, grâce à l’utilisation d’algorithmes mathématiques permettant une analyse si fine des données qu’il peuvent retrouver des variants nucléotidiques rares (quelques bases et non plus un segment entier)[11, 12]. La mise au point de techniques d’analyse dites WGS (whole-genome sequencing) a également permis d’identifier des mutations apparaissant de novo, c’est à dire non héritées depuis les parents. Conrad et al. ont d’ailleurs estimé ces mutations à environ 74 par lignée germinale (celle qui donne les ovules et les spermatozoides) [13]. Ces mutations sont particulièrement délétères et intéressantes pour les maladies sporadiques, car non soumises à la sélection naturelle qui a lieu lors du passage d’un gène d’un individu à l’autre.
Ces approches sont très complémentaires et permettent aujourd’hui de valider ce que les pathologistes voyaient sous le microscope, à savoir que toutes les cellules cancéreuses ne se ressemblent pas forcément. Plusieurs équipes ont démontré cette hétérogénéité, à la fois phénotypique et génétique [14], en ajoutant une notion évolutive. En effet, les tumeurs primaires et les métastases ne semblent pas avoir exactement le même génome et s’adaptent aux pressions externes, comme la chimiothérapie. Ces informations ont rendu possibles la caractérisation correcte des différents types de tumeurs et la prédiction de l’évolution ou de la rechute d’un cancer. Au-delà de cette aide diagnostique et préventive, la génomique permet aussi d’envisager des thérapies ultra-ciblées et personnalisées [15].
Les maladies neurodégénératives

En utilisant des échantillons sanguins, cérébro-spinaux ou cérébraux, plusieurs équipes se sont attelées au décryptage du génome des maladies neurodégénératives, et plus particulièrement Alzheimer, la plus étudiée et la plus prévalente. Grâce à leurs travaux, des gènes ont été identifiés, notamment APOE, CD33 ou EPHA1, et leurs polymorphismes semblent associés au développement de la maladie d’Alzheimer. Par exemple, CR1 (chromosome 1) et CLU (chromosome 8) ont deux loci (une zone polymorphique spécifique du gène) très fortement associés à la survenue d’une maladie d’Alzheimer [17]. En plus de ces découvertes, la génomique a aussi permis de trouver des mutations jusque là inconnues sur les gènes « classiques » de la maladie d’Alzheimer, en particulier APP (codant pour le précurseur de l’amyloide) et MAPT (codant pour la protéine Tau) (voir dossier Alzheimer).
Enfin, la contribution la plus importante de la génomique dans ce type de maladies consiste en l’étude de l’épigénome, une discipline fille de la génomique. De plus en plus, l’étude de la méthylation, du repliement et des modifications de l’ADN, ainsi que l’étude des phénomènes de régulation de l’expression génique, sont des outils capitaux pour comprendre la mise en place des pathologies neurodégénératives [18]. Pour plus d’informations, vous pouvez aller voir ce site (en anglais), qui répertorie toutes les études génomiques publiques en cours. On retrouve le même type d’études pour les maladies cardiovasculaires et les pathologies métaboliques comme le diabète. Toutes les études GWAS sont répertoriées sur ce site (en anglais) et mettent en évidence, 11 gènes pour la maladie d’Alzheimer, 42 gènes pour les maladies cardiovasculaires et 25 gènes pour le diabète, dont les polymorphismes et/ou mutations sont liés à l’apparition et/ou à la gravité de ces pathologies.
Vers une génomique anti-âge ?
La génomique peut également être utilisée pour déterminer la propension d’une cellule à devenir sénescente et plusieurs études ont déjà démontré une différence entre les phénotypes sénescents et les autres [19]. Des gènes de régulation du vieillissement ont également été identifiés, avec des polymorphismes prédisposant à une durée de vie plus ou moins longue. C’est le cas de CEBPB, un gène impliqué dans le métabolisme musculaire et dont les polymorphismes sont des facteurs de risque à la survenue des sarcopénies liées à l’âge, qui diminuent beaucoup l’espérance de vie [20].
Grâce à toutes ces recherches en génomique, des centaines de chercheurs ont pu déterminer des dénominateurs communs prédisposant aux maladies liées à l’âge. Au-delà d’une approche diagnostique, beaucoup d’entre nous espèrent voir un jour apparaitre un arsenal thérapeutique et préventif afin de prendre en charge le vieillissement dans sa globalité.
Tout notre dossier Approches « omics »
Les approches « omics » : mieux comprendre notre vieillissement
Qu’est-ce qu’il se cache derrière les approches « omics » ? Quand on parle de génomique, transcriptomique ou protéomique, à quoi s’intéresse-t-on ? Un petit guide pour mieux comprendre !
Partie 1 : Parlons peu, parlons génomique !

Difficile de ne pas s’étendre sur la génomique et toutes ses applications. C’est la plus ancienne des approches « omics » mais c’est aussi celle qui est la plus étudiée. Elle a donné naissance au concept d’épigénétique et ouvert la porte à des espoirs jusque là impossibles !
Partie 2 : La transcriptomique, une science en constante évolution.

La découverte des ARN non codants a valu un prix Nobel, c’est dire l’importance de cette discipline. La transcriptomique c’est l’ouverture d’un champ de possibles, la découverte de nouveaux mécanismes et la compréhension progressive de la régulation de la transcription.
Partie 3 : Protéomique, un meli-melo de disciplines
 La protéomique, c’est avant tout une approche multiple, prenant en compte les interactions avec d’autres disciplines, notamment la génomique, et faisant appel à des concepts intercroisés avec l’immunologie, la fonction cellulaire ou la nutrition.
La protéomique, c’est avant tout une approche multiple, prenant en compte les interactions avec d’autres disciplines, notamment la génomique, et faisant appel à des concepts intercroisés avec l’immunologie, la fonction cellulaire ou la nutrition.
Partie 4 : La métabolomique, la dernière-née des « omics »
 « Last but not least » comme diraient nos amis anglophones. La métobolomique, c’est la compréhension de réseaux de régulation complexes et la découverte quotidienne de nouveaux acteurs dans les communications entre nos cellules.
« Last but not least » comme diraient nos amis anglophones. La métobolomique, c’est la compréhension de réseaux de régulation complexes et la découverte quotidienne de nouveaux acteurs dans les communications entre nos cellules.
Références
[1] R.W. Holley, et al., Structure of a ribonucleic acid, Science, 1965;147:1462–1465
[2] Sanger, et al., Nucleotide sequence of bacteriophage phi X174 DNA, Nature 1977;265:687–695
[3] F. Sanger, A. Coulson, A rapid method for determining sequences in DNA by primed synthesis with DNA polymerase, J. Mol. Biol. 1975;94:441–448
[4] M. Maxam, W. Gilbert, A new method for sequencing DNA, Proc. Natl. Acad. Sci. U. S. A. 1977;74:560–564
[5] JA. Reuter, DV. Spacek, MP. Snyder, High-Throughput Sequencing Technologies, Molecular Cell, 2015;58(4):Pages 586-597
[6] DC. Koboldt, KM. Steinberg, DE. Larson, RK. Wilson, ER. Mardis, The Next-Generation Sequencing Revolution and Its Impact on Genomics, Cell, 2013;155(1):27-38
[7] Marchini J, Howie B. « Genotype imputation for genome-wide association studies ». Nature Reviews. Genetics. 2010;11(7):499–511
[8] Macaulay IC, Voet T. Single Cell Genomics: Advances and Future Perspectives. Maizels N, ed. PLoS Genetics. 2014;10(1):e1004126
[9] Ben-Avraham D, Muzumdar RH, Atzmon G. Epigenetic genome-wide association methylation in aging and longevity. Epigenomics. 2012;4(5):503-509
[10] Tattini L, D’Aurizio R, Magi A. Detection of Genomic Structural Variants from Next-Generation Sequencing Data. Frontiers in Bioengineering and Biotechnology. 2015;3:92
[11] C.T. Saunders, W.S. Wong, S. Swamy, J. Becq, L.J. Murray, R.K. Cheetham Strelka: accurate somatic small-variant calling from sequenced tumor-normal sample pairs, Bioinformatics, 2012;28:1811-1817
[12] K. Cibulskis, M.S. Lawrence, S.L. Carter, A. Sivachenko, D. Jaffe, C. Sougnez, S. Gabriel, M. Meyerson, E.S. Lander, G. Getz Sensitive detection of somatic point mutations in impure and heterogeneous cancer samples, Nat. Biotechnol., 2013;31:213-219
[13] D.F. Conrad, J.E. Keebler, M.A. DePrist et al., 1000 Genomes Project, Variation in genome-wide mutation rates within and between human families, Nat. Genet., 2011;43:712-714
[14] P.J. Campbell, S. Yachida, L.J. Mudie et al. The patterns and dynamics of genomic instability in metastatic pancreatic cancer, Nature, 2010;467:1109-1113
[15] Uzilov AV, Ding W, Fink MY, et al. Development and clinical application of an integrative genomic approach to personalized cancer therapy. Genome Medicine. 2016;8:627
[16] Antunez C., Boada M., Gonzalez-Perez A., Gayan J., Ramirez-Lorca R., Marin J. The membrane-spanning 4-domains, subfamily A (MS4A) gene cluster contains a common variant associated with Alzheimer’s disease. Genome Med. 2011;3:33
[17] Lambert J.C., Heath S., Even G., Campion D., Sleegers K., Hiltunen M. Genome-wide association study identifies variants at CLU and CR1 associated with Alzheimer’s disease. Nat Genet. 2009;41:1094–1099
[18] Condliffe D., Wong A., Troakes C., Proitsi P., Patel Y., Chouliaras L. Cross-region reduction in 5-hydroxymethylcytosine in Alzheimer’s disease brain. Neurobiol Aging. 2014;35:1850–1854
[19] Pilling LC, Harries LW, Powell J, Llewellyn DJ, Ferrucci L, Melzer D. Genomics and Successful Aging: Grounds for Renewed Optimism? The Journals of Gerontology Series A: Biological Sciences and Medical Sciences. 2012;67A(5):511-519
[20] Hicks GE, Shardell M, Alley DE, Miller RR, Bandinelli S, Guralnik J, Lauretani F, Simonsick EM, Ferrucci L, Absolute strength and loss of strength as predictors of mobility decline in older adults: the InCHIANTI study. J Gerontol A Biol Sci Med Sci. 2012;67(1):66-73
Dr. Marion Tible

Author/Reviewer
Auteure/Relectrice
Marion Tible has a PhD in cellular biology and physiopathology. Formerly a researcher in thematics varying from cardiology to neurodegenerative diseases, she is now part of Long Long Life team and is involved in scientific writing and anti-aging research.
More about the Long Long Life team
Marion Tible est docteur en biologie cellulaire et physiopathologie. Ancienne chercheuse dans des thématiques oscillant de la cardiologie aux maladies neurodégénératives, elle est aujourd’hui impliquée au sein de Long Long Life pour la rédaction scientifique et la recherche contre le vieillissement.
En savoir plus sur l’équipe de Long Long Life
Dr Guilhem Velvé Casquillas

Author/Reviewer
Auteur/Relecteur
Physics PhD, CEO NBIC Valley, CEO Long Long Life, CEO Elvesys Microfluidic Innovation Center
More about the Long Long Life team
Docteur en physique, CEO NBIC Valley, CEO Long Long Life, CEO Elvesys Microfluidic Innovation Center
En savoir plus sur l’équipe de Long Long Life