Vieillir l’immortel cancer
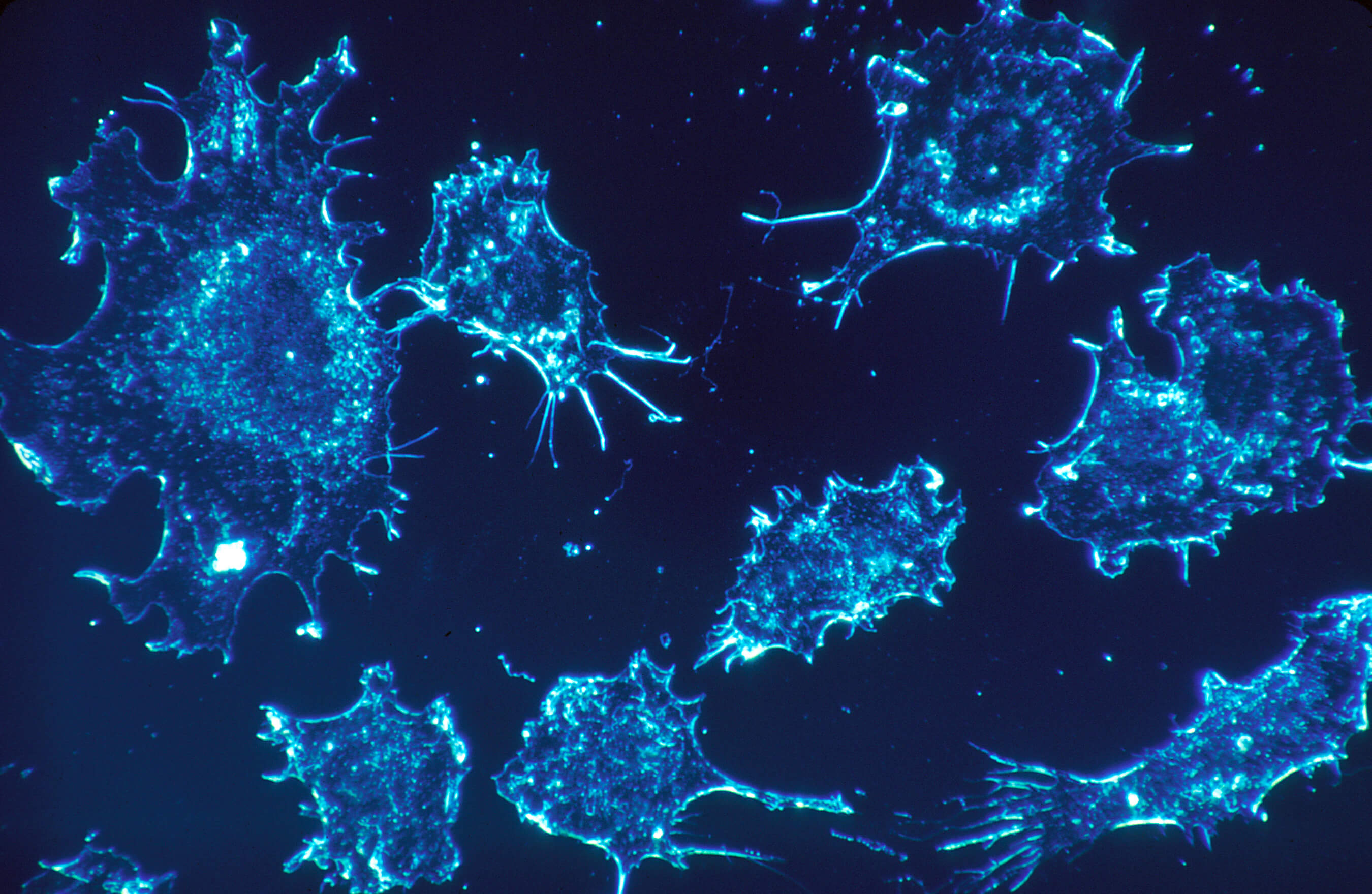
Le cancer est une maladie communément associée au vieillissement. Paradoxalement, contrairement à la plupart des cellules dans notre corps, les cellules cancéreuses ne vieillissent pas. Ce processus de vieillissement de nos cellules, menant à leur mort, permet au corps de se débarrasser des cellules après un certain temps. En effet, une vieille cellule peut avoir accumulé des dommages au cours du temps, devenant ainsi déficiente voir dangereuse. C’est le cas des cellules cancéreuses qui, elles, sont insensibles à ce mécanisme de vieillissement. Devenues invulnérables à l’écoulement du temps, elles peuvent proliférer indéfiniment, entraînant les effets que nous connaissons.
Et s’il était possible d’empêcher ces cellules de rester « jeunes » éternellement? Un regroupement de 52 chercheurs, coordonnés par Anne K. Voss et Tim Thomas, pourrait avoir réussi cet exploit. Dans leur article paru dans Nature [1] ils détaillent comment ils ont élaborés une molécule capable de faire vieillir des cellules de lymphome, une forme de cancer des cellules du sang.
KAT6A et KAT6B: la clef de la jeunesse du lymphome
Le vieillissement des cellules étant un phénomène normal, ancré dans leur ADN, le cancer doit s’armer d’outils pour y résister. Deux d’entre eux sont les protéines KAT6A et KAT6B, appartenant à la famille des histones acétyltransferases. Leur rôle est de moduler l’activité de l’ADN. Il a été montré auparavant que de très nombreux lymphomes sur-expriment ces protéines. De plus, les souris mutées pour lesquelles ces protéines sont moins actives résistent presque 4 fois plus longtemps aux lymphomes. Les chercheurs décident donc de développer une molécule capable, sans modification génétique, de bloquer l’action de ces deux protéines.
Néanmoins, c’est un défi difficile à relever. Il leur faut trouver une molécule ne se fixant que sur ces deux protéines, sans interférer avec les autres. Ce n’est pas tout, la molécule fixée peut alors avoir des effets très différents sur l’activité des protéines visées. Ainsi, elle pourrait n’avoir aucun effet, voir pire encore, rendre KAT6A et KAT6B plus active encore.
Après un long travail d’optimisation, ils parviennent à la développer. Plus encore, lorsque celle-ci est utilisée pour traiter des cellules cancéreuses en culture, elles entrent en sénescence et arrêtent alors toute forme de prolifération. Autrement dit, exposées à cette molécule, les cellules cancéreuses vieillissent.
Faire vieillir le cancer à l’intérieur de l’organisme
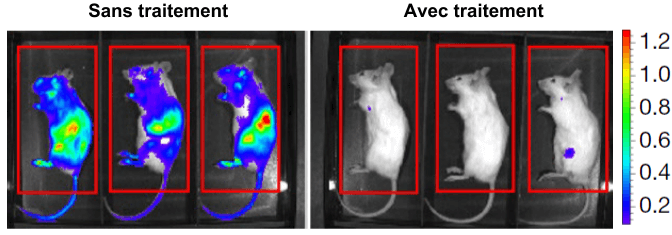
Le traitement a donc l’effet voulu sur des cellules cancéreuses en culture. Mais comment vérifier que le traitement est efficace pour lutter contre un vrai cancer? Pour cela, les chercheurs utilisent des cellules de lymphomes qu’ils injectent directement dans des souris. Ces cellules cancéreuses ont une particularité: elles émettent de la lumière par un procédé de bioluminescence. Ceci permet aux scientifiques de pouvoir observer l’évolution de la tumeur à l’intérieur même de la souris. Ils comparent alors comment le lymphome évolue suivant si la souris reçoit le traitement ou non.
Les résultats sont frappants, comme il est possible de l’observer sur la figure ci-contre, les souris recevant le traitement parviennent à juguler l’expansion de la tumeur, contrairement aux souris non traitées. Plus encore, des tests supplémentaires montrent que la rate des souris traitées, un des sièges principaux du lymphome, est presque dépourvue de cellules cancéreuses.
Ainsi, il serait possible de rappeler aux tumeurs que le temps passe et qu’elles aussi, elles vieillissent. En l’empêchant de proliférer, étape indispensable à son développement, cette nouvelle molécule agit comme une véritable barrière contre le lymphome. Et si Anne K. Voss et Tim Thomas venaient de découvrir le traitement anti-cancer de demain?
Références:
[1] Jonathan B. Baell, David J. Leaver, …Tim Thomas. Inhibitors of histone acetyltransferases KAT6A/B induce senescence and arrest tumour growth. Nature (2018)
Baptiste Tesson

Author
Auteur
Baptiste is studying biology at the École Normale Supérieure de Lyon and bioengineering at the École Polytechnique Fédérale de Lausanne. He worked on the optimization of Cas9 as a tool for genome editing and on the emergence of blood stem cells in the zebrafish. He currently works on the patterning of the muscles, also in the zebrafish. He plans on doing a PhD in developmental biology.
More about the Long Long Life team
Baptiste étudie la biologie à l’École Normale Supérieure de Lyon et la bioingénierie à l’École Polytechnique Fédérale de Lausanne. Il a travaillé sur l’optimisation de la protéine Cas9 comme outil de modification de génomes et sur le développement des cellules souches du sang chez le poisson zèbre et travaille actuellement sur la mise en place des muscles chez le même animal. Il projette de réaliser un doctorat axé vers le développement animal.
En savoir plus sur l’équipe de Long Long Life